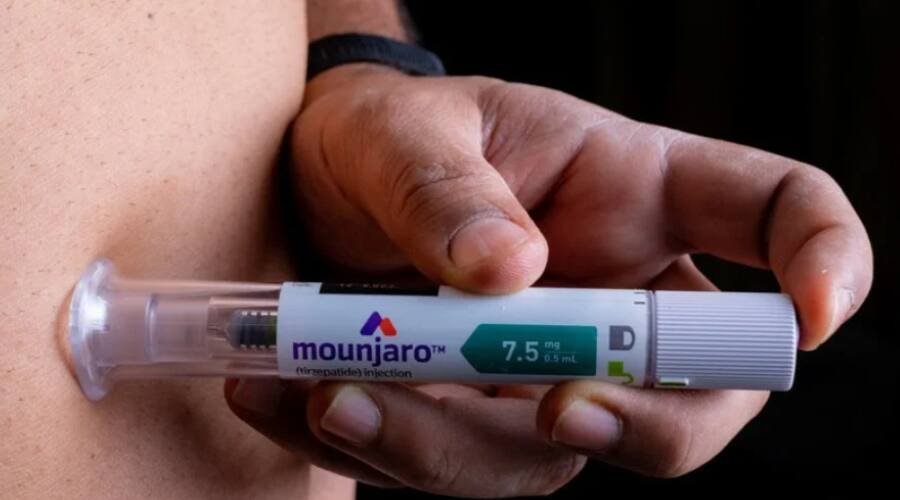
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou o uso da tirzepatida, conhecida comercialmente como Mounjaro, para tratar diabetes tipo 2 em crianças e adolescentes de 10 a 17 anos. Esta decisão amplia o uso do medicamento, que já era permitido para adultos e controle de peso em casos específicos.
Mounjaro: pioneirismo no uso pediátrico
Com a nova autorização, o Mounjaro se torna o primeiro medicamento da classe dos agonistas duplos dos receptores GIP/GLP-1 a ser liberado para uso pediátrico no Brasil. Esses fármacos atuam em hormônios que regulam a glicose e o apetite, ajudando a diminuir os níveis de açúcar no sangue e, em alguns casos, o peso corporal.
Impacto no tratamento de jovens
No Brasil, cerca de 213 mil adolescentes vivem com diabetes, além de mais de 1,4 milhão com pré-diabetes. A nova indicação permite que médicos considerem a tirzepatida como alternativa quando outras terapias não são eficazes no controle da glicemia. No entanto, o tratamento deve ser personalizado e monitorado por especialistas, dado o perfil vulnerável e em desenvolvimento dos pacientes.
Base científica da aprovação
A autorização pela Anvisa foi fundamentada em um estudo clínico internacional de fase 3, publicado na revista Lancet. Os resultados mostraram que os efeitos adversos em crianças e adolescentes foram similares aos já conhecidos, principalmente sintomas gastrointestinais como náusea, diarreia e vômito, geralmente leves a moderados e mais comuns no início do tratamento. Não houve registros de hipoglicemia grave.
Considerações finais
A aprovação do Mounjaro para jovens representa um avanço significativo no tratamento do diabetes tipo 2 em uma faixa etária crítica. A decisão reforça a importância de tratamentos inovadores e personalizados para condições crônicas que afetam cada vez mais jovens em todo o mundo.
Para mais informações sobre o estudo e os efeitos do medicamento, consulte a publicação na revista Lancet.
Fonte: portalpe10.com.br